Morbus Parkinson
Morbus Parkinson ist eine chronische, progressive neurodegenerative Erkrankung, die vorwiegend das motorische System betrifft. Die Erkrankung wurde erstmals 1817 von James Parkinson beschrieben und ist durch Symptome wie Tremor, Rigidität, Bradykinesie und posturale Instabilität gekennzeichnet. Der Verlust dopaminerger Neuronen in der Substantia nigra führt zu einem Dopaminmangel im Striatum, was die typischen motorischen Störungen verursacht.
Definition
Morbus Parkinson ist eine chronische, neurodegenerative Erkrankung des Zentralnervensystems, die durch den Verlust von Dopamin-produzierenden Nervenzellen im Gehirn, insbesondere in der Substantia nigra, verursacht wird. Dies führt zu motorischen Symptomen wie Zittern, Muskelsteifheit, verlangsamten Bewegungen und Gleichgewichtsstörungen. Weitere Symptome können psychische Veränderungen, Schlafstörungen und autonome Dysfunktionen umfassen. Parkinson schreitet fort und ist derzeit nicht heilbar, aber die Symptome können durch Medikamente und Therapien gelindert werden.
Epidemiologie
Morbus Parkinson ist nach Alzheimer die zweithäufigste neurodegenerative Erkrankung. Die Prävalenz liegt bei etwa 0,3% der Gesamtbevölkerung und steigt auf 1% bei Personen über 60 Jahre. Männer sind etwas häufiger betroffen als Frauen. Die Inzidenz beträgt etwa 8 bis 18 Fälle pro 100.000 Personen pro Jahr, wobei die Zahl in den letzten Jahrzehnten aufgrund der alternden Bevölkerung zunimmt.
Pathophysiologie
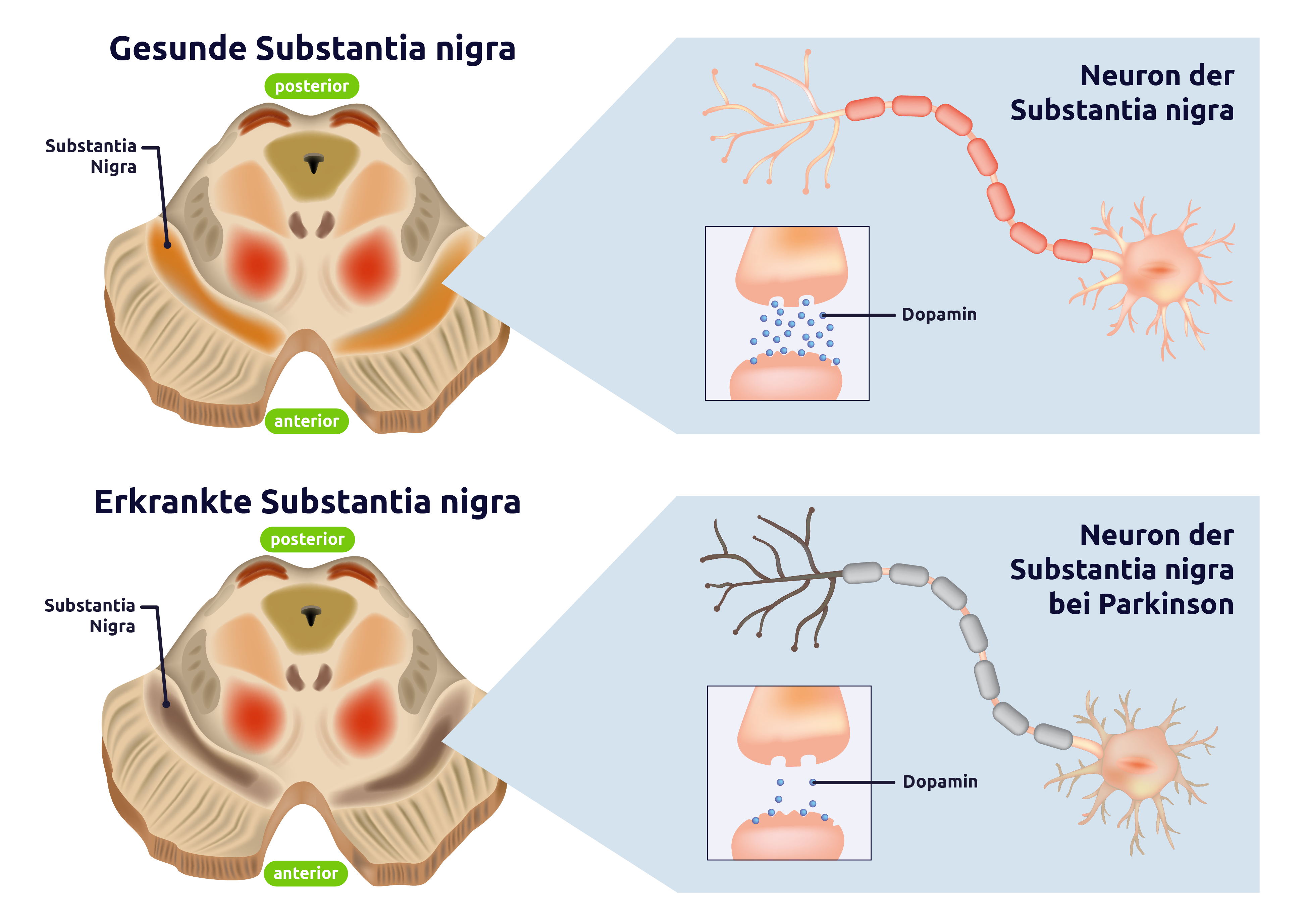
Die primäre pathologische Veränderung bei Morbus Parkinson ist der Verlust von dopaminergen Neuronen in der Substantia nigra pars compacta. Diese Neuronen sind für die Produktion von Dopamin verantwortlich, einem Neurotransmitter, der entscheidend für die Regulation von Bewegungen ist.
Hauptkomponenten der Pathophysiologie:
- Lewy-Körperchen
➜ diese intrazellulären eosinophilen Einschlusskörperchen bestehen hauptsächlich aus aggregiertem α-Synuclein und sind ein Kennzeichen der Krankheit. Sie werden in den verbleibenden Neuronen gefunden und sind mit neuronaler Dysfunktion und Tod assoziiert. - Mitochondriale Dysfunktion
➜ Störungen in den Mitochondrien führen zu erhöhtem oxidativem Stress, was zur Degeneration der Neuronen beiträgt. Defekte in den mitochondrialen DNA-Polymerasen und die Akkumulation von mitochondrialer DNA-Schäden sind ebenfalls mit Parkinson assoziiert. - Genetische Faktoren
➜ Mutationen in Genen wie SNCA (α-Synuclein), LRRK2, Parkin, PINK1 und DJ-1 sind mit familiären Formen der Krankheit assoziiert. Diese genetischen Faktoren spielen eine wichtige Rolle bei der Pathogenese und bieten Einblicke in die molekularen Mechanismen der Erkrankung. - Neuroinflammation
➜ Entzündliche Prozesse im Gehirn, vermittelt durch Mikroglia und Astrozyten, tragen zur Neurodegeneration bei. Chronische Entzündung führt zu weiteren Schäden an den Neuronen.
Symptome
Die klinischen Symptome von Morbus Parkinson lassen sich in motorische und nicht-motorische Symptome unterteilen.
Motorische Symptome
Morbus Parkinson ist primär durch motorische Symptome gekennzeichnet, die durch den Verlust dopaminerger Neuronen in der Substantia nigra verursacht werden. Diese Symptome beeinflussen die Bewegungsfähigkeit und Koordination und sind für die Diagnose der Krankheit von zentraler Bedeutung.
Tremor
- Ruhetremor
➜ Der Ruhetremor ist das typischste Merkmal von Morbus Parkinson. Er tritt in Ruhe auf und wird oft als „Pillendrehertremor“ bezeichnet, weil die Fingerbewegungen an das Drehen einer Tablette zwischen Daumen und Zeigefinger erinnern. Der Tremor ist meist asymmetrisch und betrifft häufig die Hände, kann aber auch die Beine, das Kinn oder die Lippen betreffen. Der Tremor verschwindet oder vermindert sich bei Bewegung und wird durch Stress oder emotionale Belastungen verstärkt.
Rigidität
- Muskelsteifigkeit
➜ Rigidität bezieht sich auf eine erhöhte Muskelspannung, die zu einer Steifigkeit und Widerstand gegen passive Bewegungen führt. Dies kann zu Muskelverspannungen und Schmerzen führen. Bei der Untersuchung zeigt sich ein gleichmäßiger Widerstand während der gesamten Bewegung, was als „Bleirohr-Phänomen“ bezeichnet wird. - Zahnradphänomen
➜ Ein weiteres charakteristisches Merkmal der Rigidität ist das „Zahnradphänomen“, bei dem die Bewegung des betroffenen Gliedes ruckartig und nicht glatt verläuft. Dies kann durch passive Bewegungen der Gliedmaßen während der klinischen Untersuchung festgestellt werden.
Bradykinesie
- Verlangsamung der Bewegung
➜ Bradykinesie ist eine Verlangsamung der Bewegungen und eines der Hauptmerkmale von Morbus Parkinson. Sie äußert sich in einer verminderten Bewegungsamplitude und -geschwindigkeit. - Erschwerte Initiierung von Bewegungen
➜ Patienten haben Schwierigkeiten, Bewegungen zu initiieren, was zu einer Verzögerung bei der Durchführung einfacher Aufgaben führen kann. Dies kann sich auf alltägliche Aktivitäten wie Gehen, Schreiben oder Anziehen auswirken. - Mikrografie
➜ Ein häufiges Zeichen der Bradykinesie ist die Mikrografie, bei der die Handschrift des Patienten klein und unleserlich wird. - Gesichtsmaske
➜ Verminderte Mimik, was zu einem starren, maskenhaften Gesichtsausdruck führt.
Posturale Instabilität
- Gleichgewichtsstörungen
➜ Posturale Instabilität bezieht sich auf Probleme mit dem Gleichgewicht und der Haltung, die zu einer erhöhten Sturzgefahr führen. Dies ist besonders in den späteren Stadien der Krankheit ausgeprägt. - Verlust der Reflexe zur Haltungsstabilisierung
➜ Patienten verlieren die Fähigkeit, ihre Haltung automatisch zu korrigieren, wenn sie aus dem Gleichgewicht geraten. - Retropulsion und Propulsion
➜ Patienten können eine Tendenz zum Rückwärtsfallen (Retropulsion) oder Vorwärtsfallen (Propulsion) zeigen.
Weitere motorische Symptome
- Gangstörungen
➜ Typischerweise haben Patienten einen schlurfenden Gang mit kurzen, langsamen Schritten. Das Einfrieren der Bewegung („Freezing“) kann auftreten, insbesondere beim Starten oder Drehen. - Dystonie
➜ Einige Patienten entwickeln abnorme, schmerzhafte Muskelkontraktionen, die zu verdrehten Haltungen führen. - Dyskinesien
➜ Bei Langzeittherapie mit Levodopa können unwillkürliche, überschüssige Bewegungen auftreten, die als Dyskinesien bekannt sind.
Nicht-motorische Symptome
Neuropsychiatrische Symptome
Depression
- Häufigkeit: Depression ist eine der häufigsten nicht-motorischen Symptome bei Parkinson und betrifft etwa 40-50% der Patienten.
- Symptome: Anhaltende Traurigkeit, Verlust des Interesses an Aktivitäten, Veränderungen im Schlaf- und Essverhalten, Konzentrationsschwierigkeiten, Hoffnungslosigkeit.
- Behandlung: Antidepressiva (SSRIs, SNRIs), kognitive Verhaltenstherapie, Psychotherapie.
Angststörungen
- Häufigkeit: Etwa 30-40% der Patienten leiden unter Angststörungen.
- Symptome: Generalisierte Angst, Panikattacken, soziale Phobie.
- Behandlung: Anxiolytika, SSRIs, kognitive Verhaltenstherapie.
Psychosen
- Häufigkeit: Psychotische Symptome wie Halluzinationen und Wahnvorstellungen treten bei etwa 20-40% der Patienten auf, oft als Nebenwirkung der dopaminergen Medikation.
- Symptome: Visuelle Halluzinationen, Paranoia, Wahnvorstellungen.
- Behandlung: Anpassung der dopaminergen Medikation, Antipsychotika wie Clozapin und Quetiapin (die weniger extrapyramidale Nebenwirkungen haben).
Demenz
- Häufigkeit: Parkinson-Demenz entwickelt sich bei etwa 30-40% der Patienten, insbesondere in den späteren Stadien der Krankheit.
- Symptome: Gedächtnisverlust, Schwierigkeiten beim Planen und Organisieren, langsames Denken, Verwirrtheit.
- Behandlung: Cholinesterase-Hemmer (Rivastigmin), symptomatische Behandlung und Unterstützung durch kognitive Therapien.
Autonome Symptome
Orthostatische Hypotonie
- Häufigkeit: Tritt bei etwa 20-50% der Parkinson-Patienten auf.
- Symptome: Schwindel, Benommenheit, Ohnmacht beim Aufstehen aus dem Sitzen oder Liegen.
- Behandlung: Erhöhte Flüssigkeits- und Salzaufnahme, Tragen von Kompressionsstrümpfen, Medikamente wie Midodrin und Fludrocortison.
Blasenfunktionsstörungen
- Häufigkeit: Etwa 30-40% der Patienten erleben Blasenfunktionsstörungen.
- Symptome: Dranginkontinenz, häufiges Wasserlassen, nächtlicher Harndrang.
- Behandlung: Blasentraining, anticholinerge Medikamente, Betmiga (Mirabegron).
Gastrointestinale Symptome
- Häufigkeit: Häufige Symptome sind Verstopfung und verzögerte Magenentleerung (Gastroparese).
- Symptome: Seltener Stuhlgang, Bauchschmerzen, Übelkeit, Erbrechen.
- Behandlung: Ballaststoffreiche Diät, Laxantien, Prokinetika.
Sexualstörungen
- Häufigkeit: Erektile Dysfunktion und verminderte Libido sind häufige Beschwerden.
- Symptome: Schwierigkeiten, eine Erektion zu erreichen oder aufrechtzuerhalten, verminderte sexuelle Lust.
- Behandlung: PDE-5-Hemmer (Sildenafil), Testosteron-Ersatztherapie.
Sensorische Symptome
Schmerzen
- Häufigkeit: Bis zu 80% der Patienten berichten über Schmerzen, die von muskuloskelettalen Schmerzen bis hin zu neuropathischen Schmerzen reichen können.
- Symptome: Schulterschmerzen, Nackensteifheit, Brennen, Kribbeln.
- Behandlung: Analgetika, Antikonvulsiva, Physiotherapie, Massage.
Vermindertes Geruchsempfinden (Hyposmie)
- Häufigkeit: Hyposmie tritt bei etwa 70-90% der Parkinson-Patienten auf und kann eines der frühesten Symptome sein.
- Symptome: Verlust des Geruchssinns, der oft Jahre vor den motorischen Symptomen auftritt.
- Behandlung: Keine spezifische Behandlung, jedoch kann eine Geruchstrainingstherapie hilfreich sein.
Schlafstörungen
REM-Schlaf-Verhaltensstörung (RBD)
- Häufigkeit: Tritt bei etwa 30-50% der Parkinson-Patienten auf.
- Symptome: Ausagieren von Träumen, was zu Verletzungen führen kann.
- Behandlung: Clonazepam, Melatonin.
Schlaflosigkeit
- Häufigkeit: Sehr häufig bei Parkinson-Patienten.
- Symptome: Schwierigkeiten beim Einschlafen und Durchschlafen, frühes Erwachen.
- Behandlung: Schlafhygiene, kognitive Verhaltenstherapie für Schlaflosigkeit (CBT-I), Medikamente wie Melatonin, Zolpidem.
Tagesschläfrigkeit
- Häufigkeit: Betrifft etwa 20-50% der Patienten.
- Symptome: Übermäßige Schläfrigkeit während des Tages, ungewolltes Einschlafen.
- Behandlung: Anpassung der Medikation, stimulierende Medikamente wie Modafinil.
Diagnose
Die Diagnose von Morbus Parkinson basiert primär auf klinischen Kriterien und einer gründlichen Anamnese. Es gibt keine spezifischen diagnostischen Tests, aber verschiedene Untersuchungen können zur Unterstützung der Diagnose beitragen.
Klinische Kriterien
In Deutschland orientieren sich die klinischen Kriterien für die Diagnose von Morbus Parkinson an internationalen Standards, wie den UK Parkinson’s Disease Society Brain Bank Kriterien. Diese Kriterien wurden entwickelt, um die Diagnose von Parkinson-Erkrankungen zu standardisieren und zu präzisieren. Die Diagnosestellung erfolgt in der Regel durch Neurologen, die eine gründliche Anamnese und klinische Untersuchung durchführen. Hier sind die wichtigsten diagnostischen Kriterien zusammengefasst:
Stufe 1: Klinische Diagnose eines Parkinson-Syndroms
Für die klinische Diagnose eines Parkinson-Syndroms muss Bradykinesie plus mindestens eines der folgenden Symptome vorliegen:
- Bradykinesie
➜ Verlangsamung der Bewegungen und verminderte Bewegungsamplitude. - Ruhetremor
➜ typischerweise ein Ruhetremor, der bei Bewegung des betroffenen Körperteils nachlässt. - Rigor
➜ erhöhter Muskeltonus, der sich als Steifigkeit und Widerstand gegen passive Bewegungen zeigt. - Posturale Instabilität
➜ Gleichgewichtsstörungen und erhöhte Sturzgefahr, die nicht durch primäre visuelle, vestibuläre, zerebellare oder propriozeptive Dysfunktionen erklärt werden kann.
Stufe 2: Ausschlusskriterien für Parkinson
Ein Parkinson-Syndrom wird ausgeschlossen, wenn eines der folgenden Kriterien zutrifft:
- Symptomfreies Intervall
➜ eine klare Symptomfreie Zeit zwischen der Exposition eines verursachenden Medikaments oder Toxins und dem Beginn der Symptome. - Bilaterale Symptome von Beginn an
➜ ohne asymmetrischen Beginn. - Kleinhirnbeteiligung
➜ Hinweise auf zerebelläre Dysfunktionen. - Frühe schwere autonome Dysfunktion
➜ schwere orthostatische Hypotonie oder Inkontinenz früh im Krankheitsverlauf. - Frühe schwere Demenz
➜ deutliche kognitive Beeinträchtigungen innerhalb eines Jahres nach Beginn der motorischen Symptome. - Babinski-Zeichen
➜ das Vorliegen pathologischer Reflexe, die auf eine Pyramidenbahn-Läsion hinweisen. - Unzureichendes Ansprechen auf Levodopa
➜ fehlendes Ansprechen auf eine adäquate Levodopa-Therapie.
Stufe 3: Unterstützende Kriterien
Mindestens drei der folgenden unterstützenden Kriterien sollten für eine definitive Diagnose von Morbus Parkinson erfüllt sein:
- Einseitiger Beginn
➜ Symptome beginnen auf einer Körperseite. - Ruhetremor
➜ deutlicher Ruhetremor vorhanden. - Progression
➜ langsame Progression der Erkrankung. - Persistierende Asymmetrie
➜ Symptomstärke bleibt auf der initial betroffenen Körperseite stärker. - Gutes Ansprechen auf Levodopa
deutliche Verbesserung der Symptome durch Levodopa-Therapie. - Levodopa-induzierte Dyskinesien
➜ Auftreten von Dyskinesien durch Langzeit-Levodopa-Therapie. - Ansprechen auf Apomorphin-Test
➜ positive Reaktion auf den Apomorphin-Test, welcher die dopaminerge Funktion überprüft.
Anamnese und klinische Untersuchung
Die Anamnese sollte detailliert die Krankheitsgeschichte, familiäre Vorbelastungen und mögliche Expositionen gegenüber Umweltfaktoren erfassen. Die klinische Untersuchung umfasst eine sorgfältige Bewertung der motorischen und nicht-motorischen Symptome sowie der neurologischen Funktion. Besondere Aufmerksamkeit wird auf die Beurteilung von Tremor, Rigor, Bradykinesie und posturaler Instabilität gelegt.
Bildgebung
- DaTSCAN (Dopamin-Transporter-Szintigraphie)
➜ kann zur Differenzierung zwischen Morbus Parkinson und anderen Parkinsonismen beitragen, indem der Dopamintransporter in den Basalganglien dargestellt wird. - MRT
➜ wird verwendet, um andere neurologische Erkrankungen auszuschließen und strukturelle Hirnveränderungen zu beurteilen.
Differentialdiagnosen
- Essentieller Tremor
➜ ein gutartiger Tremor ohne die anderen motorischen Merkmale von Parkinson. - Atypische Parkinson-Syndrome
➜ Multisystematrophie (MSA), progressive supranukleäre Blickparese (PSP), kortikobasale Degeneration (CBD). - Medikamenten-induzierte Parkinsonismen
➜ durch Medikamente wie Antipsychotika oder Calciumkanalblocker verursacht.
Therapien
Die Behandlung von Morbus Parkinson zielt darauf ab, die Symptome zu lindern und die Lebensqualität der Patienten zu verbessern. Eine Heilung der Erkrankung ist derzeit nicht möglich.
Pharmakologische Therapie
- Levodopa
➜ Das wirksamste Medikament zur Symptomkontrolle. Es wird häufig in Kombination mit Carbidopa oder Benserazid (sogenannten Decarboxylasehemmern) verabreicht, um die periphere Metabolisierung zu verhindern und die Bioverfügbarkeit im Gehirn zu erhöhen. - Dopaminagonisten
➜ Medikamente wie Pramipexol, Ropinirol und Rotigotin wirken direkt auf die Dopaminrezeptoren und können als Monotherapie in frühen Stadien oder in Kombination mit Levodopa in fortgeschrittenen Stadien verwendet werden. - MAO-B-Hemmer
➜ Selegilin und Rasagilin verlangsamen den Dopaminabbau im Gehirn und können die Wirkung von Levodopa verstärken. - COMT-Hemmer
➜ Entacapon und Tolcapon verlängern die Wirkung von Levodopa, indem sie dessen Abbau hemmen. - Anticholinergika
➜ Zur Kontrolle von Tremor, jedoch begrenzt durch Nebenwirkungen wie Verwirrtheit, Mundtrockenheit und Harnverhalt. - Amantadin
➜ Kann zur Reduktion von Dyskinesien beitragen, die durch Levodopa verursacht werden.
Bei fortgeschrittenem Morbus Parkinson kann der Einsatz einer Levodopa-Pumpe (auch L-Dopa-Pumpe genannt) sinnvoll sein. Hierbei erfolgt eine kontinuierliche Aufnahme des Wirkstoffes L-Dopa direkt über den Dünndarm.
Chirurgische Therapie
- Tiefe Hirnstimulation (THS)
➜ ein Verfahren, bei dem Elektroden in bestimmte Hirnregionen implantiert werden, um die motorischen Symptome zu kontrollieren. THS ist besonders wirksam bei Patienten mit fortgeschrittenem Morbus Parkinson und motorischen Fluktuationen. - Pallidotomie und Thalamotomie
➜ chirurgische Ablationen bestimmter Hirnregionen, die bei ausgewählten Patienten in Betracht gezogen werden können.
Nicht-pharmakologische Therapie
- Physiotherapie
➜ zur Verbesserung der Mobilität, Balance und Muskelkraft. Übungen zur Sturzprävention und Gangtraining sind besonders wichtig. - Ergotherapie
➜ Unterstützung bei alltäglichen Aktivitäten und Anpassungen im häuslichen Umfeld zur Erhöhung der Selbstständigkeit. - Logopädie
➜ Behandlung von Sprach- und Schluckstörungen, die häufig bei Parkinson-Patienten auftreten. - Psychologische Unterstützung
➜ Bewältigung von Depressionen, Angstzuständen und kognitiven Veränderungen durch psychologische Beratung und Therapie.
Komplikationen
- Motorische Fluktuationen
- On-Off-Phänomene und Dyskinesien, die mit langfristiger Levodopa-Therapie auftreten. Diese Fluktuationen können durch Anpassung der Medikation oder durch THS gemindert werden.
- Demenz
- Entwicklung einer Parkinson-Demenz bei etwa 30-40% der Patienten. Diese ist oft schwer zu behandeln und verschlechtert die Lebensqualität erheblich.
- Psychosen
- Halluzinationen und Wahnvorstellungen, oft verstärkt durch dopaminerge Medikamente. Diese erfordern häufig eine Anpassung der Medikation und können antipsychotische Medikamente wie Clozapin erfordern.
- Schlafstörungen
- REM-Schlaf-Verhaltensstörung, Schlaflosigkeit und Tagesschläfrigkeit beeinträchtigen die Lebensqualität erheblich und erfordern spezifische Behandlungsstrategien.
Prävention und Lebensstil
Obwohl eine Prävention von Morbus Parkinson derzeit nicht möglich ist, können bestimmte Lebensstiländerungen das Fortschreiten der Krankheit verlangsamen und die Lebensqualität verbessern.
- Regelmäßige Bewegung
- kann die motorische Funktion und Lebensqualität verbessern. Aktivitäten wie Gehen, Tanzen, Tai Chi und Yoga sind besonders vorteilhaft.
- Gesunde Ernährung
- eine ausgewogene Ernährung mit ausreichender Zufuhr von Antioxidantien, Omega-3-Fettsäuren und Ballaststoffen kann das allgemeine Wohlbefinden fördern.
- Soziale Unterstützung
- Teilnahme an Selbsthilfegruppen und soziale Interaktionen können psychische Belastungen reduzieren und die Lebensqualität verbessern.
- Kognitive Übungen
- Mentale Stimulation durch Lesen, Puzzles und soziale Aktivitäten kann helfen, kognitive Funktionen zu erhalten.
Forschung und zukünftige Entwicklungen
Die Forschung zu Morbus Parkinson ist intensiv und zielt darauf ab, bessere diagnostische Methoden, neue therapeutische Ansätze und möglicherweise Heilungsmethoden zu finden.
- Biomarker
- Identifikation von Biomarkern zur frühzeitigen Diagnose und Überwachung des Krankheitsverlaufs. Diese könnten in Blut, Liquor oder mittels bildgebender Verfahren nachgewiesen werden.
- Gentherapie
- Erforschung der Möglichkeiten zur Reparatur oder zum Ersatz defekter Gene, die zur Entwicklung von Morbus Parkinson beitragen.
- Stammzelltherapie
- Potenzial zur Erneuerung und Reparatur geschädigter Neuronen durch Transplantation von dopaminergen Vorläuferzellen.
- Immuntherapie
- Einsatz von Antikörpern gegen α-Synuclein, um die Bildung von Lewy-Körperchen zu verhindern oder zu reduzieren.
- Neuroprotektive Strategien
- Erforschung von Substanzen, die die Degeneration dopaminerger Neuronen verlangsamen oder stoppen können.
Pflege bei Parkinson
Die Pflege bei Parkinson umfasst die Unterstützung bei täglichen Aktivitäten, Mobilitätsübungen, Medikamentenmanagement und emotionale Betreuung. Wesentlich sind gezielte Physiotherapie, Ergotherapie und Sprachtherapie, um Beweglichkeit und Kommunikationsfähigkeiten zu fördern. Eine individuelle, patientenzentrierte Pflegeplanung ist entscheidend, um die Lebensqualität zu verbessern und die Selbstständigkeit zu erhalten.
Zusammenfassung
Morbus Parkinson ist eine komplexe neurodegenerative Erkrankung, die eine multidisziplinäre Herangehensweise erfordert. Durch die Kombination aus pharmakologischer, chirurgischer und nicht-pharmakologischer Therapie kann die Lebensqualität der Patienten erheblich verbessert werden. Fortschritte in der Forschung bieten Hoffnung auf bessere Diagnose- und Behandlungsmöglichkeiten in der Zukunft.
Bei diesem Artikel handelt es sich um ein Gesundheitsthema. Er dient weder der Selbstdiagnose noch ersetzt er eine Diagnose durch einen Arzt. Bitte zusätzlich den Hinweis zu Gesundheitsthemen beachten!
Quellen
- Haupt, W. F., & Gouzoulis-Mayfrank, E. (2016). Neurologie und Psychiatrie für Pflegeberufe (W. F. Haupt & E. Gouzoulis-Mayfrank, Hrsg.; 11. Aufl.). Thieme.
- Jankovic, J. (2008). Parkinson’s disease: clinical features and diagnosis. Journal of Neurology, Neurosurgery & Psychiatry, 79(4), 368-376.
- Kalia, L. V., & Lang, A. E. (2015). Parkinson’s disease. The Lancet, 386(9996), 896-912.
- Poewe, W., Seppi, K., Tanner, C. M., Halliday, G. M., Brundin, P., Volkmann, J., … & Lang, A. E. (2017). Parkinson disease. Nature Reviews Disease Primers, 3(1), 1-21.
- Obeso, J. A., Stamelou, M., Goetz, C. G., Poewe, W., Lang, A. E., Weintraub, D., … & Marsden, C. D. (2017). Past, present, and future of Parkinson’s disease: a special essay on the 200th anniversary of the shaking palsy. Movement Disorders, 32(9), 1264-1310.
- Fahn, S., & Sulzer, D. (2004). Neurodegeneration and neuroprotection in Parkinson disease. NeuroRx, 1(1), 139-154.

