Virchow-Trias
Die Virchow-Trias ist ein fundamentaler Begriff in der Medizin, insbesondere in der Hämatologie und Angiologie, der die drei Hauptfaktoren beschreibt, die zur Entstehung von Thrombosen beitragen. Die Thrombose ist die Bildung eines Blutgerinnsels in einem Blutgefäß, was zu schwerwiegenden Komplikationen wie Embolien führen kann. Die Virchow-Trias umfasst Störungen des Blutflusses (Stase), Veränderungen der Blutzusammensetzung (Hyperkoagulabilität) und Schäden an der Gefäßwand (Endothelschaden).
Historischer Hintergrund
Rudolf Virchow (1821-1902) war einer der einflussreichsten Pathologen seiner Zeit und gilt als Begründer der modernen Pathologie. Er hat entscheidende Beiträge zum Verständnis vieler Krankheiten geleistet, darunter Thrombosen. Virchow erkannte, dass die Entstehung eines Thrombus nicht nur auf eine einzige Ursache zurückgeführt werden kann, sondern das Zusammenspiel mehrerer Faktoren notwendig ist. Diese Erkenntnisse wurden später als Virchow-Trias bekannt und haben das Fundament für die moderne Thromboseforschung gelegt.
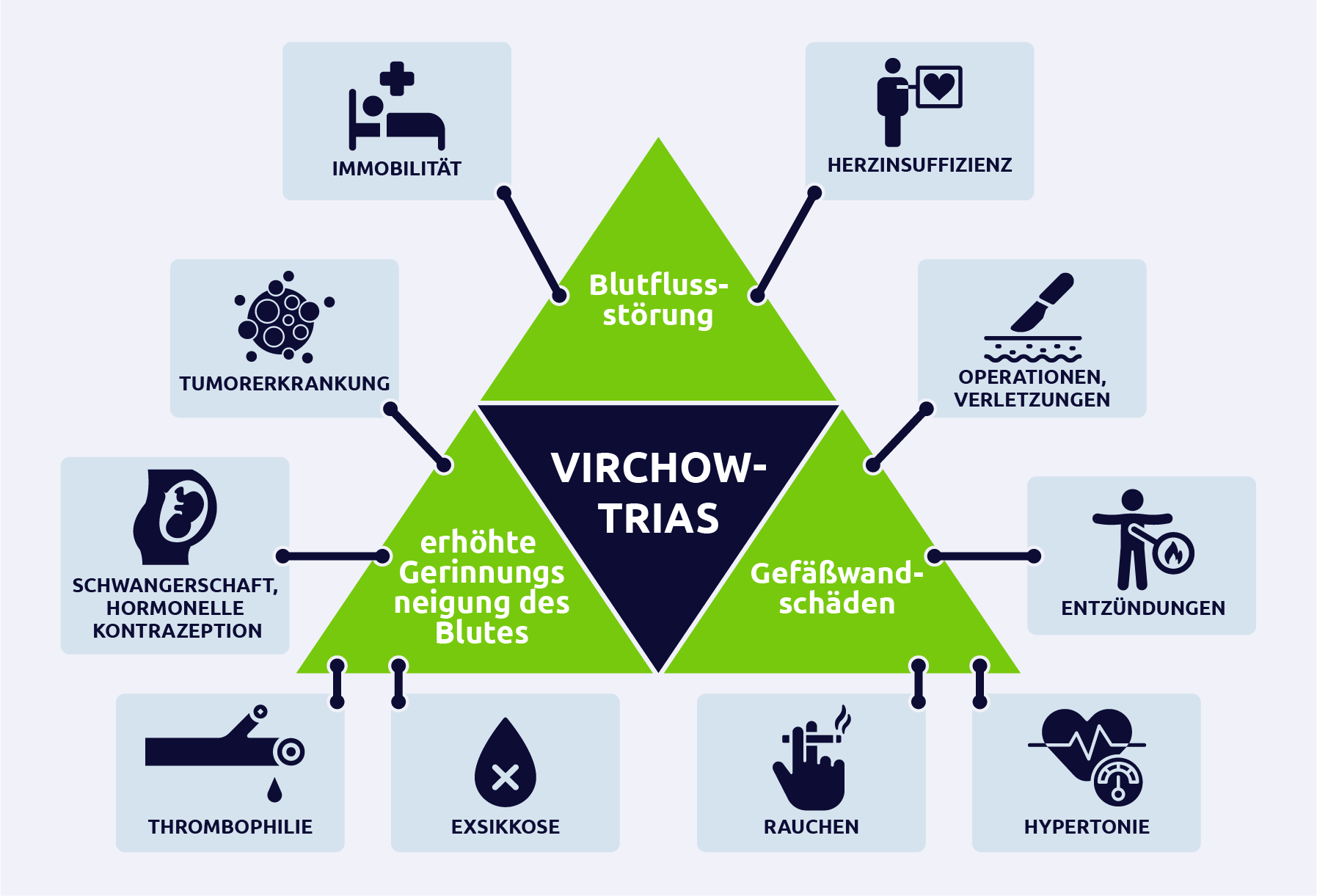
1. Stase (Blutflussstörung)
Stase, oder die Verlangsamung des Blutflusses, ist ein kritischer Faktor für die Thrombusbildung. Normalerweise hilft der kontinuierliche Blutfluss, die Bildung von Gerinnseln zu verhindern, indem er Thrombozyten und Gerinnungsfaktoren gleichmäßig verteilt und gerinnungshemmende Faktoren wie Heparin über das Endothel freisetzt. Verschiedene Bedingungen können jedoch zu einer Stase führen, darunter:
- Immobilität
- Langzeitimmobilisierung, wie sie bei Bettlägerigkeit, langen Flugreisen oder Gipsverbänden vorkommt, führt zu einer signifikanten Verlangsamung des venösen Rückflusses, insbesondere in den unteren Extremitäten.
- Herzinsuffizienz
- Ein unzureichender Herzoutput kann zu einer systemischen Stase führen, was die Wahrscheinlichkeit einer Thrombose erhöht.
- Venöse Obstruktion
- Bedingungen wie Tumore oder Schwangerschaft können Druck auf die Venen ausüben und den Blutfluss behindern.
Medizinisches Personal sollte daher bei Patienten mit diesen Risikofaktoren besonders aufmerksam sein und präventive Maßnahmen wie Mobilisation, Kompressionsstrümpfe oder medikamentöse Prophylaxe in Betracht ziehen.
2. Hyperkoagulabilität (erhöhte Gerinnungsneigung)
Hyperkoagulabilität bezeichnet eine erhöhte Neigung des Blutes zu gerinnen. Diese kann durch genetische Faktoren oder erworbene Bedingungen verursacht werden:
- Genetische Faktoren
- Thrombophilien wie Faktor-V-Leiden-Mutation, Prothrombin-Mutation oder Mangel an natürlichen Gerinnungshemmern (Protein C, Protein S, Antithrombin III) erhöhen das Thromboserisiko.
- Erworbene Faktoren
- Verschiedene klinische Zustände können eine Hyperkoagulabilität verursachen, darunter:
- Malignität: Krebspatienten haben ein erhöhtes Risiko für venöse Thromboembolien (VTE) aufgrund von tumorbedingten Prokoagulantien.
- Schwangerschaft: Physiologische Veränderungen während der Schwangerschaft führen zu einer erhöhten Gerinnungsbereitschaft, um postpartale Blutungen zu minimieren.
- Medikamente: Hormonelle Kontrazeptiva und Hormonersatztherapien sind bekannte Risikofaktoren für Thrombosen.
- Verschiedene klinische Zustände können eine Hyperkoagulabilität verursachen, darunter:
Bei Patienten mit bekannten Risikofaktoren für Hyperkoagulabilität sollten prophylaktische Maßnahmen und eine engmaschige Überwachung in Betracht gezogen werden.
3. Endothelschaden (Schäden an der Gefäßwand)
Schäden am Endothel der Blutgefäße spielen eine zentrale Rolle in der Thrombusbildung. Das Endothel wirkt normalerweise antithrombotisch, indem es Substanzen wie Prostacyclin und Stickstoffmonoxid freisetzt, die die Thrombozytenaggregation hemmen. Endothelschäden können durch verschiedene Mechanismen verursacht werden:
- Trauma oder chirurgische Eingriffe
- Direkte Verletzungen der Blutgefäße durch Operationen oder Traumata können die Integrität des Endothels beeinträchtigen und die Thrombusbildung fördern.
- Entzündliche Prozesse
- Zustände wie Atherosklerose, Infektionen oder Autoimmunerkrankungen führen zu einer Entzündung und Schädigung des Endothels, was die Thrombozytenaktivierung und Gerinnselbildung begünstigt.
- Chronische Erkrankungen
- Hypertonie und Diabetes mellitus sind bekannte Faktoren, die langfristig zu Endothelschäden führen können.
Praktische Anwendungen und Präventivmaßnahmen
Zur Prävention von Thrombosen sollten folgende Strategien in der klinischen Praxis berücksichtigt werden:
- Risikostratifizierung
- Regelmäßige Bewertung des Thromboserisikos bei allen Patienten unter Berücksichtigung der Virchow-Trias.
- Pharmakologische Prophylaxe
- Einsatz von Antikoagulanzien wie Heparin, Warfarin oder neuen oralen Antikoagulanzien (NOAKs) bei Risikopatienten.
- Mechanische Prophylaxe
- Anwendung von Kompressionsstrümpfen oder intermittierenden pneumatischen Kompressionsgeräten zur Förderung des venösen Rückflusses.
- Patientenedukation
- Aufklärung der Patienten über Risikofaktoren, Symptome von Thrombosen und präventive Maßnahmen, insbesondere bei bevorstehenden Operationen oder längerer Immobilität.
Ein fundiertes Verständnis der Virchow-Trias und ihrer praktischen Implikationen ermöglicht es medizinischem Personal, Thrombosen effektiv vorzubeugen und zu behandeln, wodurch die Patientensicherheit und -gesundheit erheblich verbessert werden können.
Fallbeispiel zur Virchow-Trias
Patientenprofil
- Name: Frau Müller
- Alter: 65 Jahre
- Anamnese: Adipositas, Hypertonie, Diabetes mellitus Typ 2
- Aktueller Zustand: Vor drei Tagen einer Hüftgelenksersatzoperation unterzogen
Klinische Präsentation
- Symptome
➜ Schmerzen und Schwellung im rechten Unterschenkel, leichte Atemnot - Vitalparameter
➜ Puls 98 bpm, Blutdruck 140/85 mmHg, Atemfrequenz 22/min, Temperatur 37,4°C
Diagnostische Maßnahmen
- Duplex-Sonographie der Beinvenen
➜ Bestätigung einer tiefen Venenthrombose (TVT) im rechten Unterschenkel - D-Dimer-Test
➜ Es werden erhöhte Werte festgestellt - CT-Angiographie
➜ Ausschluss einer Lungenembolie
Analyse der Virchow-Trias
- Stase
➜ Frau Müller war nach der Hüftoperation längere Zeit immobilisiert. Bettlägerigkeit und eingeschränkte Mobilität führten zu einer verminderten venösen Rückfluss im rechten Bein. - Hyperkoagulabilität
➜ Als übergewichtige Patientin mit Diabetes und Hypertonie hat Frau Müller mehrere Risikofaktoren, die zu einer erhöhten Gerinnungsneigung führen. Zudem könnten postoperative Faktoren und mögliche entzündliche Reaktionen die Gerinnungsneigung weiter gesteigert haben. - Endothelschäden
➜ Die chirurgische Intervention selbst stellt einen mechanischen Stress für die Gefäße dar, was zu mikrotraumatischen Endothelschäden führen kann. Die operative Manipulation und die postoperative Inflammation tragen ebenfalls zur Gefäßschädigung bei.
Therapie und Management
- Medikamentös
➜ Einleitung einer Antikoagulationstherapie mit niedermolekularem Heparin, gefolgt von einer oralen Antikoagulation. - Mechanisch
➜ Verwendung von Kompressionsstrümpfen zur Unterstützung des venösen Rückflusses. - Mobilisation
➜ Frühzeitige Mobilisation unter Anleitung eines Physiotherapeuten, um die Stase zu minimieren. - Monitoring
➜ Regelmäßige Überwachung der Gerinnungsparameter und klinischen Symptome zur Anpassung der Therapie.
Prävention
- Aufklärung der Patientin über die Bedeutung von Mobilisation und die Risiken einer erneuten Thrombose.
- Langfristige Risikoreduktion durch Gewichtskontrolle, Blutzuckermanagement und Blutdruckeinstellung.
Zusammenfassung
Die Virchow-Trias bleibt ein grundlegendes Konzept in der Medizin und bietet eine wertvolle Grundlage für das Verständnis der Thrombosepathogenese. Durch die Berücksichtigung der Faktoren Stase, Hyperkoagulabilität und Endothelschäden können medizinisches Personal und Forscher bessere Strategien zur Prävention und Behandlung von Thrombosen entwickeln und so die Patientensicherheit und -gesundheit verbessern.
Quellen
- Faller, A., & Schünke, M. (2016). Der Körper des Menschen: Einführung in Bau und Funktion (A. Faller & M. Schünke, Hrsg.; 17. Aufl.). Thieme.
- Bauer, K.A. and Lip, G.Y.H., 2011. Hypercoagulability: too many tests, too many policies? Journal of Thrombosis and Haemostasis, 9(7), pp. 1249-1251.
- Di Nisio, M., van Es, N. and Büller, H.R., 2016. Deep vein thrombosis and pulmonary embolism. The Lancet, 388(10063), pp.3060-3073.
- Geerts, W.H., Bergqvist, D., Pineo, G.F., Heit, J.A., Samama, C.M., Lassen, M.R. and Colwell, C.W., 2008. Prevention of venous thromboembolism: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest, 133(6 Suppl), pp.381S-453S.
- Kearon, C., Akl, E.A., Ornelas, J., Blaivas, A., Jimenez, D., Bounameaux, H., Huisman, M., King, C.S., Morris, T.A., Sood, N. and Stevens, S.M., 2016. Antithrombotic therapy for VTE disease: CHEST guideline and expert panel report. Chest, 149(2), pp.315-352.
- Morris, T.A. and Marsh, J.J., 2014. The pathogenesis of venous thrombosis: a critical review. Hemostasis and Thrombosis: Basic Principles and Clinical Practice, pp.379-388.
- Raskob, G.E., Angchaisuksiri, P., Blanco, A.N., Buller, H., Gallus, A., Hunt, B.J., Hylek, E.M., Kakkar, A., Konstantinides, S.V., McCumber, M. and Ozaki, Y., 2014. Thrombosis: a major contributor to global disease burden. Arteriosclerosis, Thrombosis, and Vascular Biology, 34(11), pp.2363-2371.
- Virchow, R., 1856. Phlogose und Thrombose im Gefäßsystem. Gesammelte Abhandlungen zur Wissenschaftlichen Medizin, pp.458-636.
- Wolberg, A.S., Aleman, M.M., Leiderman, K. and Machlus, K.R., 2012. Procoagulant activity in hemostasis and thrombosis: Virchow’s triad revisited. Anesthesia & Analgesia, 114(2), pp.275-285.